Kuzey Carolina Üniversitesi (UNC) Tıp Fakültesi ve UNC Eshelman Eczacılık Fakültesi araştırmacıları, hızlı ilerleyen ve son derece ölümcül bir beyin kanseri türü olarak bilinen “glioblastoma”nın tedavisi için yeni yöntem geliştirdi.
Çalışmada, laboratuvarlarda yaygın olarak kullanılan kemoterapi ilacı Temozolomid (TMZ) ile EdU adlı kimyasalın birlikte kullanılmasının, çeşitli preklinik glioblastoma modellerinde eşi görülmemiş sağkalım ve kanser gerilemesi sağladığı ortaya kondu. Makale, Proceedings of the National Academy of Sciences (PNAS) dergisinde 31 Aralık 2025’te yayınlandı.
UNC Lineberger Comprehensive Cancer Center üyesi ve Nobel ödüllü biyokimyacı Aziz Sancar, üniversitenin bültenindeki açıklamasında, “Bir dizi klinik öncesi çalışma yaptık. Bazılarında yalnızca EdU, bazılarında yalnızca TMZ, bazılarında ise ikisini birlikte kullandık. Temel fikir basit. TMZ ile EdU’yu birlikte kullandığımızda ilacın tümörleri yok edebildiğini ve ölümü önleyebildiğini gördük.” dedi.
Glioblastoma, son derece hızlı büyüyen ve ölümcül bir beyin kanseri türü. Günümüzde hastaların yalnızca yaklaşık yüzde 7’si tanıdan sonra beş yıldan fazla yaşayabiliyor, diğerleri hayatlarını kaybediyor. Yoğun araştırmalara rağmen, glioblastoma tedavisinde kullanılan yöntemler ise son 20 yıldır aynı kaldı.
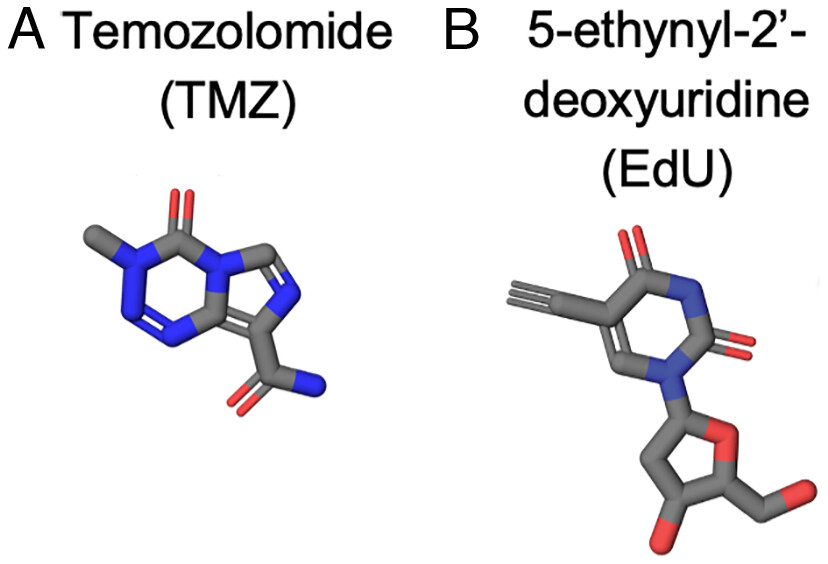
Deneylerde kullanılan Temozolomid (TMZ), radyoterapi ile birlikte kullanılan ve glioblastoma için FDA tarafından onaylanmış tek kemoterapi ilacı. Ancak standart tedavi her hastada etkili olmuyor ve tedavi kesildiğinde tümörler daha agresif şekilde geri dönüyor.
Glioblastoma’nın tedavisi neden zor?
Prof. Dr. Aziz Sancar ve ekibinin üzerinde çalıştığı söz konusu beyin kanserinin tedavisini zorlaştıran başlıca nedenler ise; beyin dokusu içinde çok hızlı büyümesi, hayati beyin bölgelerine zarar verme riski nedeniyle tümörün tamamen çıkarılmasının zor olması ve çok sayıda genetik mutasyona sahip olması şeklinde açıklanıyor. Bu nedenle, “herkese uyan tek tedavi” yaklaşımı neredeyse imkansız hale geliyor.
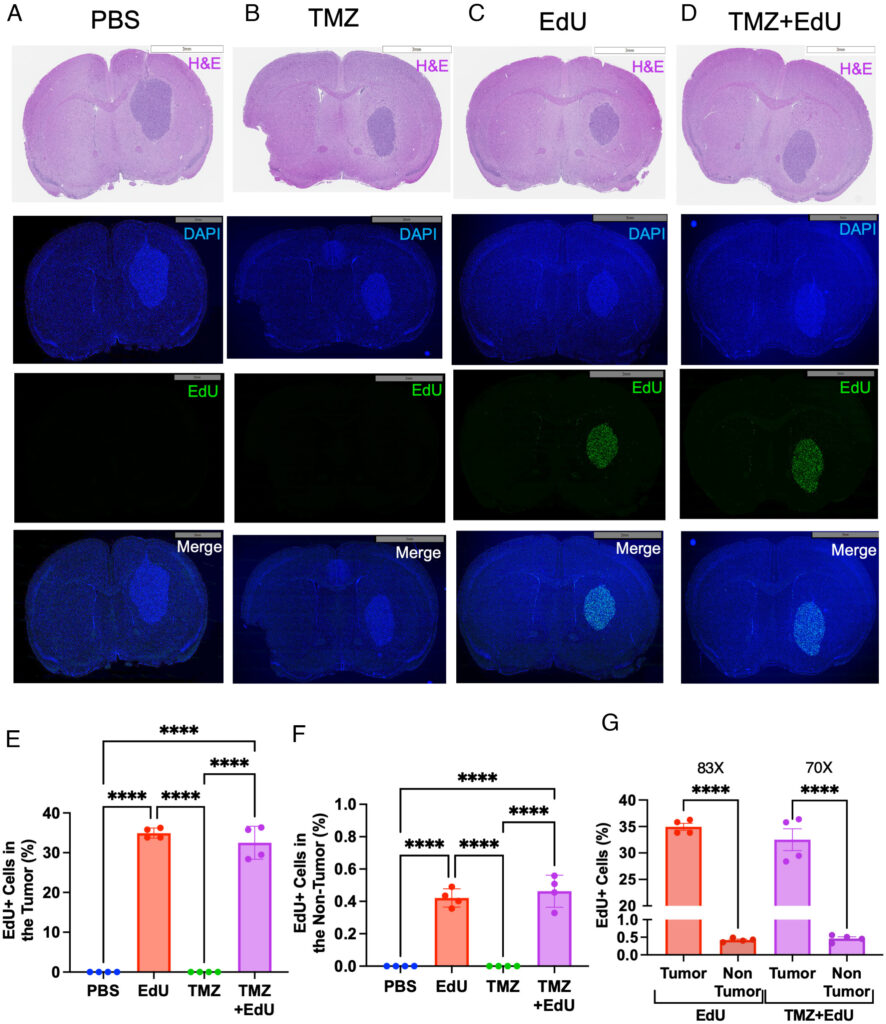
Öte yandan, Sancar ve laboratuvarındaki bilim insanları uzun yıllardır daha etkili tedavi yaklaşımlarını arıyor. Hatta 2025’in ekim ayında, yaygın olarak laboratuvarlarda kullanılan EdU (5-Ethynyl-2′-deoxyuridine) adlı kimyasalın glioblastoma tedavisinde ciddi bir potansiyele sahip olduğunu keşfettiler. Yayımlanan çalışmada, glioblastoma hastalarından çıkarılan gerçek tümör dokularında, EdU’nun beyne geçebildiği, tümör içindeki hücreleri öldürdüğü ve sağlıklı beyin dokusuna zarar vermediği gösterildi.
Bulguların ardından Sancar’ın laboratuvarı, EdU’nun TMZ ile birlikte kullanımını değerlendiren yeni bir kombinasyon tedavisi çalışması başlattı.
Tümörler yok oldu, en az 250 gün yaşadılar
Prof. Dr. Sancar ve ekibi, geliştirdikleri ilacı farklı dozlarda üç farklı glioblastoma hücre hattında test etti: U87, GBM8 ve LN229. Bu hücre hatları, geçmişte glioblastoma tanısı almış hastalardan elde edilmiş olup günümüzde laboratuvar ortamında, test tüplerinde ve canlı modellerde (örneğin farelerde) çoğaltılarak kullanılıyor.
Hücre hattı, bir hastadan veya dokudan alınan hücrelerin laboratuvar ortamında uzun süre çoğaltılarak sürekli kullanılabilir hali. Kanser araştırmalarında, hastalığı kontrollü ve tekrarlanabilir biçimde incelemek için kullanılıyor.
Araştırmacılar, kanser büyümesini ve küçülmesini net biçimde izleyebilmek için her hücre hattına biyolüminesan bir kimyasal enjekte etti.
U87 tümörlü fare modellerinde şu sonuçlar elde edildi: Kontrol grubu (tedavi edilmeyenler) 30 gün içinde öldü. Sadece EdU verilenler yaklaşık 45 gün yaşadı. Sadece TMZ verilenler ise yaklaşık 53 gün hayatta kaldı. Ancak tedaviler birleştirildiğinde (200 mg/kg EdU + 5 mg/kg TMZ), 23. günde tüm kanser dokusunun tamamen ortadan kalktığı gözlendi. Farelerin hepsi, çalışmanın sonuna kadar, yani 250 günü aşan süre boyunca yaşamaya devam etti. Kısacası iyileştiler.
Aynı yaklaşım GBM8 hücre hattı içeren modellerde de test edildi. Kombinasyon tedavisi alan tüm fareler —ister 1 mg/kg TMZ + 200 mg/kg EdU, ister 5 mg/kg TMZ + 200 mg/kg EdU olsun— 170 gün sonunda halen hayattaydı ve tümörden arınmışlardı.
Güvenli mi?
Araştırmacılar ayrıca tedavinin ince bağırsak, böbrek, dalak, karaciğer, akciğer ve kan gibi dokular üzerinde zararlı etkiler oluşturup oluşturmadığını da inceledi.
Tedavi yalnızca ince bağırsak, dalak ve kanda hafif değişikliklere yol açtı. Etkiler, standart kemoterapilerde görülen tipik yan etkilere benziyordu.
U87 ve GBM8 çalışmalarında, TMZ ve EdU’nun birlikte kullanımında “sinerjik etki” saptandı. Sinerji, iki tedavinin birlikte kullanıldığında, tek tek kullanımlarından daha güçlü etki göstermesi anlamına geliyor. Sancar bu durumu şöyle açıkladı:
“Sinerjik bir kombinasyon, bir artı birin üç etmesi gibidir. Aditif etki ise bir artı birin iki etmesi demektir. Diğer üç tümörde etki aditifti; hücreler yine öldü ama sinerji yoktu.”
Araştırmacılar, cerrahi işlem sonrası hastalardan alınan canlı glioblastoma tümör örnekleri üzerinde de aynı tedaviyi test etti.
UNC’deki Screening Live Cancer Explants (SLiCE) Core Facility’de kullanılan özgün tümör modeli, hasta tümör hücreleri ile canlı sağlıklı beyin dokusunu birlikte içeren, gerçek bir tümörü en iyi temsil eden modellerden biri. Deneyde bu model kullanıldı. Model üzerinde dört farklı hasta glioblastoması test edildi: Birinde güçlü sinerjik etki, üçünde additif etki gözlendi.
Sıra insan deneylerinde
Prof. Dr. Aziz Sancar’ın laboratuvarı artık insan klinik çalışmaları yürütmeyi hedefliyor ve FDA onayı almayı.
Sancar’ın laboratuvarı, günümüzde hastalarda en sık görülen glioblastoma türü olan EGFR-mutant glioblastoma üzerine ek çalışmalar yapıyor. Tüm hasta örneklerinin aynı yanıtı vermemesi, kişiselleştirilmiş tedavilerin ve hasta kaynaklı dokuların önemini bir kez daha ortaya koyuyor. Bu yüzden, her hastanın tümörüne özel tedavi stratejileri geliştirmeye odaklanıyorlar.
Sancar’ın laboratuvarında doktora öğrencisi Hümeyra Kaanoğlu, ortak birinci yazarı olduğu makaleyi, “Hastaya özgü farklı kombinasyon tedavilerine karşı farklı hassasiyetler saptadık. Glioblastoma tedavisinde kişiselleştirilmiş kombinasyon yaklaşımları, bu yıkıcı hastalık için acilen ihtiyaç duyulan alternatifleri sunabilir.” sözleriyle değerlendirdi.
Kaynaklar: 2N News, PNAS, UNC bülteni

