Yapısal biyoloji teknikleri, bakterilerin bağışıklık silahı olan CapE enzimini nasıl aktive ettiğini ortaya koydu.
Bakterilerde bağışıklık mekanizmasının sırrı
Çin Bilimler Akademisi Biyofizik Enstitüsü ile Pekin Teknoloji Enstitüsünden araştırmacıların ortak yürüttüğü bir çalışma, bakterilerin virüslere karşı kendilerini nasıl savunduklarını ortaya koyan önemli bir bağışıklık mekanizmasını aydınlattı. 8 Mayıs 2025’te Cell dergisinde yayınlanan araştırmaya göre, bakteriler enfeksiyon durumunda hücre zarlarını hedef alarak virüsleri etkisiz hale getiren bir bağışıklık yanıtı başlatıyor.
Çalışmanın merkezinde, bakterilerdeki CBASS (cyclic oligonucleotide-based anti-phage signaling system) adı verilen bağışıklık sistemi yer alıyor. CBASS, bakterilerin virüs saldırılarına karşı geliştirdiği bir tür “doğuştan gelen bağışıklık” savunması. Bu sistemin ilginç yönlerinden biri, prokaryotlar (yani bakteriler gibi çekirdeksiz canlılar) ile ökaryotlar (çekirdekli hücreye sahip canlılar) arasında korunmuş olması. Bu da CBASS’in bağışıklık sistemlerinin evrimi açısından önemli bir yapı taşı olduğunu gösteriyor.
CBASS sistemi aktive olduğunda, CDNs (cyclic dinucleotides) adı verilen halkasal nükleotid molekülleri üretiliyor. Bu moleküller, bağışıklık yanıtını başlatan sinyal görevi görüyor. Ancak şimdiye kadar bu sinyallerin bağışıklık sisteminin etkili silahlarını nasıl devreye soktuğu tam olarak bilinmiyordu.
Yapısal biyoloji teknikleriyle çözüm
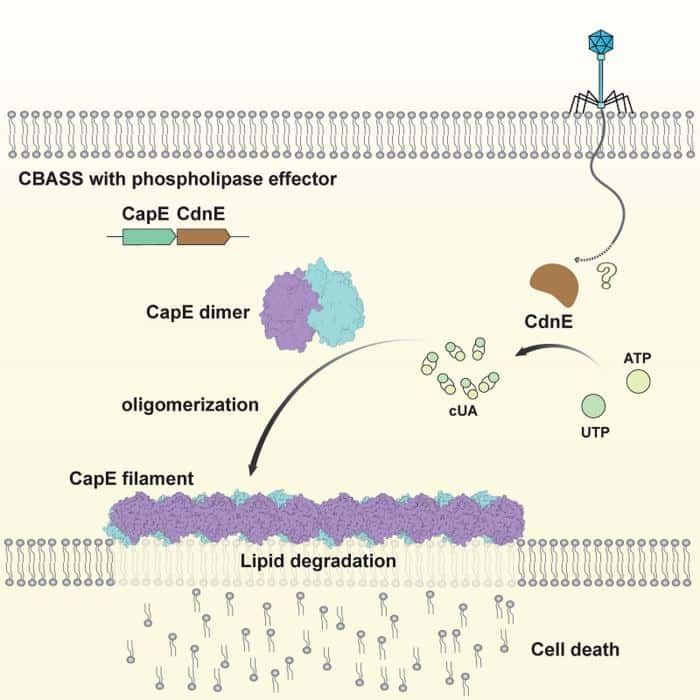
Araştırmacılar bu sorunun cevabını bulmak için CBASS sisteminin önemli bir bileşeni olan CapE adlı enzimi inceledi. CapE, bir tür fosfolipaz enzimi. Yani hücre zarındaki fosfolipidleri keserek zar bütünlüğünü bozan ve hücrenin kendini feda etmesini sağlayan bir mekanizmayı tetikliyor.
CapE’nin nasıl aktive olduğunu anlamak için araştırma ekibi, kriyo-elektron mikroskobu (cryo-EM) ve X-ışını kristalografisi gibi ileri düzey yapısal biyoloji tekniklerini kullandı. Bu tekniklerle CapE’nin üç farklı yapısal durumunu görüntülediler: inaktif (etkisiz) dimer hali, CDNs ile bağlandığı zaman aldığı yeni form ve substrat benzeri bir molekülle bağlandığında oluşan katalitik yapı.
Elde edilen yapılar, CapE’nin CDNs’e bağlandığında büyük bir yapısal dönüşüm geçirdiğini gösteriyor. Bu dönüşüm sırasında enzimin aktif bölgesi ortaya çıkıyor ve CapE, uzun filamentler (ipliksi yapılar) oluşturacak şekilde polimerleşiyor. Bu filamentler, hücre zarındaki fosfolipidlere saldıran bir platform gibi çalışıyor. Böylece bakteri, virüsle enfekte olmuş hücreyi yok ederek virüsün yayılmasını engelliyor.
Yapılan genetik değişiklik deneyleriyle (mutagenez) hem filament oluşumunun hem de CapE’nin enzimatik aktivitesinin bu bağışıklık tepkisinin başarısı için gerekli olduğu kanıtlandı.
Genel bağışıklık prensiplerine ışık tutuyor
Araştırmacılar, bu çalışma ile CDNs moleküllerinin nasıl etkili bağışıklık yanıtlarına yol açtığını moleküler düzeyde ilk kez detaylı biçimde gösterdi. Ayrıca, filament oluşumunun yalnızca bakterilere özgü bir mekanizma olmadığını, çeşitli canlı türlerinde bağışıklık sistemlerinde ortak bir strateji olarak kullanıldığını vurguluyorlar.
Bu bulgular, hem bakterilerin bağışıklık sisteminin işleyişine dair bilgimizi derinleştiriyor hem de bu tür mekanizmaların gelecekte biyoteknolojik uygulamalarda, örneğin antibiyotik direncine karşı yeni stratejiler geliştirmede, kullanılmasının yolunu açıyor.
Kaynak: Eurekalert